- AI 는 심음 청진으로 심부전을 찾아낼 수 있을까?
- 전기적 심율동전환을 받은 심방세동 환자에서 카페인 함유 커피를 매일 섭취한 군은 커피·카페인 금욕군에 비해 심방세동/심방조동 재발 위험이 낮았다
- SGLT-2 inhibitor는 심방세동 도자절제술 후 조기 재발 예방에 효과가 있을까?
- Endothelial AGO1, 염증과 지질대사 이상을 하나로 잇는 새로운 심혈관질환 기전
- DAPA-EAT 연구: 무증상 심부전 환자에서 SGLT2 억제제를 투여하면 심장주위 지방이 줄까?
- ATTR-CM 치료, 새로운 전환점이 될 수 있을까? — Coramitug의 2상 무작위 대조시험 결과
- CAVIAR trial: 심장이식 후 alirocumab을 추가 투여는 CAV 진행을 억제하지 못한다.
- KARDIA-3: 조절되지 않는 고혈압과 높은 심혈관 위험을 가진 환자에서 Zilebesiran의 무작위 배정 임상시험
- 무증상 중증 대동맥 판막 협착증에서 조기 수술과 보존적 치료의 장기 성적 비교: RECOVERY 연구의 최종 결과
- PCI후 아스피린 즉시중단 및 강력한 P2Y12억제제 단독요법의 유효성 평가
- 약물 용출 스텐트 삽입 후 1년이 지난 심방 세동 환자에서 NOAC 단독 용법으로 충분한가?
KARDIA-3: 조절되지 않는 고혈압과 높은 심혈관 위험을 가진 환자에서 Zilebesiran의 무작위 배정 임상시험
KARDIA-3: A Randomized Trial of Zilebesiran in Patients with Uncontrolled Hypertension and High Cardiovascular Risk
연구요약
KARDIA-3 연구는 고혈압이 조절되지 않는 환자 중 심혈관질환을 이미 가지고 있거나 고위험군(ASCVD 10년 위험도 ≥15%)을 대상으로, RNA 간섭(RNAi) 치료제 zilebesiran의 혈압 강하 효과와 안전성을 평가한 다국가, 무작위배정, 이중눈가림, 위약대조 2상 임상시험이다.
Zilebesiran은 간에서 angiotensinogen(AGT) 생성을 억제하여 레닌-안지오텐신-알도스테론계(RAAS)의 가장 상위 단계를 차단하는 기전으로 작용하며, 피하주사 6개월 1회로 지속적인 혈압 조절이 가능하도록 설계된 신약이다.
본 연구는 eGFR에 따라 두 코호트로 구성되었다.
Cohort A: eGFR ≥ 45 mL/min/1.73 m² (효능 및 안전성 평가, ESC 2025에서 발표)
Cohort B: eGFR 30–44 mL/min/1.73 m² (안전성 중심 평가)
대상자는 평균 진료실 수축기혈압(SBP) 140–170 mmHg, 24시간 ABPM 130–170 mmHg이면서 항고혈압제 2–4제(이뇨제 또는 CCB 포함)를 복용 중인 환자였으며, 혈중 K+ ≤ 4.8 mEq/L을 만족해야 했다.
본 연구의 1차 평가지표(primary endpoint)는 3개월 시점에서의 평균 진료실 수축기혈압(SBP) 변화였으며, 2차 평가지표(secondary endpoints)는 6개월 시점에서의 안전성(이상반응, 고칼륨혈증, eGFR 감소, 저혈압 등)이었다.
Cohort A(eGFR ≥45 mL/min/1.73m²) 에서는 zilebesiran 300mg 및 600mg 투여군 모두 위약 대비 약 –9mmHg 수준의 평균 SBP 감소를 보였다. 다만, 복수 비교(multiplicity) 보정 이후에는 통계적 유의성이 유지되지 않았다. 전반적인 이상반응은 대부분 경미하거나 일시적이었으며, 고칼륨혈증, 신기능 저하, 저혈압의 발생 빈도는 모두 낮았다.
Cohort B(eGFR 30–44 mL/min/1.73m²)에서는 평균 연령이 70세였고 여성의 비율이 약 40%였으며, 전체의 약 70% 이상이 세 가지 이상의 항고혈압제를 복용 중이었다. Zilebesiran 투여군에서 이상반응은 50–67%의 환자에서 발생하였으나 대부분 경미하거나 일시적이었다. 중대한 이상반응은 전체의 6.6%에서 보고되었으며, 약물과 관련된 심각한 이상반응은 담낭염으로 입원 및 복강경 담낭절제술을 시행한 1건뿐이었고, 해당 환자는 완전히 회복되었다. 사망 사례는 1건(심정지)이 보고되었으나, 연구자 판단에 따라 약물과의 관련성은 없는 것으로 평가되었다.
혈중 칼륨 농도 5.5mmol/L를 초과하는 고칼륨혈증은 13.2%의 환자에서 관찰되었으며, 대부분 일시적이었고 입원이나 투석 치료가 필요한 경우는 없었다. eGFR이 30% 이상 감소한 사례는 전체의 9.2%에서 확인되었으나 대부분 추적 검사에서 회복되었다. 저혈압 관련 이상사건은 임상적으로 의미 있는 수준의 발생이 보고되지 않았다. 3개월 시점에서 측정한 평균 SBP 변화는 위약 대비 약 –8~–13 mmHg의 감소로, CKD 환자군에서도 일관된 혈압강하 효과가 관찰되었다.
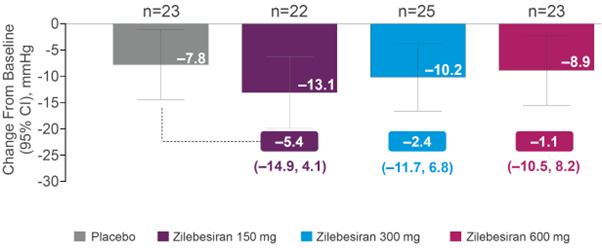
그림1. Placebo-adjusted change from baseline in office SBP at Month 3 in Cohort B
임상적 의의
KARDIA-3 연구는 RNAi 기반 RAAS 억제제가 기존 다제요법에도 혈압이 조절되지 않는 환자에서 지속적이고 장기적인 혈압강하를 달성할 수 있음을 입증한 최초의 무작위 대조 시험이다. 특히 만성콩팥병(CKD, eGFR 30–44) 환자군에서도 고칼륨혈증·신기능 저하·저혈압의 위험이 모두 낮게 유지되어, 신기능 저하 환자에서도 안전하게 사용 가능한 장기 지속형 치료제임이 확인되었다. 전체 2상 데이터는 300 mg 6개월 1회 용량이 안전성과 효능의 균형을 보이는 최적 용량임을 시사하였으며, 이를 기반으로 현재 ZENITH 3상 CV Outcome Trial(N≈11,000명, NCT07181109) 이 진행 중이다.
참고문헌
1) Pagidipati N et al. KARDIA-3: A Randomized Trial of Zilebesiran Versus Placebo on Top of Standard Care for Patients with Hypertension and Established Cardiovascular Disease or High Cardiovascular Risk. Presented at AHA 2025, Chicago, IL.
2) Alnylam Pharmaceuticals Press Release. Zilebesiran Demonstrates Sustained BP Reduction and Favorable Safety Profile in KARDIA-3 Trial. Cambridge, MA; 2025.
3) European Society of Cardiology Congress 2025 (Abstract No. BP-4512).

