- 안정적인 심근경색 환자에서 베타차단제를 중지하는 것은 SMART DECISION이다
- 경피적 관상동맥 중재술 후 만성관리 시점에 단일 항혈소판제 요법으로서의 아스피린 대 클로피도그렐 비교: HOST-EXAM 임상시험의 10년 추적 관찰 연구
- KARDINAL: 조절되지 않는 고혈압 환자에서 Tonlamarsen의 효능 및 안전성 평가를 위한 2상 무작위 배정 임상시험
- Ez-PAVE trial + 죽상경화성 심혈관질환 환자에서 LDL 콜레스테롤 집중 목표 치료
- SURViV 연구: 승모판 생체인공판막 기능 이상에서 Valve-in-Valve 시술 대 재수술의 무작위 대조연구
- TAVI전 routine PCI와 보존적(deferral)전략의 비교(PRO-TAVI trial)
- 중증 삼첨판 역류 환자에서 경피적 삼첨판 edge-to-edge repair의 2년 임상결과: TRI-FR 무작위 연구
- 혈전색전증 예방이 필요한 심방세동 환자에서 좌심방이 폐색술은 항응고제를 대체할 수 있는가?
- 유전자 치료, 치명적인 유전성 심근증의 대안이 될 수 있을까?
- 전기적 심율동전환을 받은 심방세동 환자에서 카페인 함유 커피를 매일 섭취한 군은 커피·카페인 금욕군에 비해 심방세동/심방조동 재발 위험이 낮았다
- HFpEF에 동반된 복합 폐모세혈관전후 폐고혈압에서 Sotatercep가 새로운 치료 옵션이 될 수 있을까? CADENCE 2상 연구
- SURPASS-CVOT의 Cardiorenal Outcomes: 죽상동맥경화증이 있는 당뇨병 환자에서 Tirzepatide를 투여하면 Dulaglutide에 비하여 심장, 신장 관련 예후가 개선된다.
- AI 망막 분석은 안과 검진에서 심혈관 고위험군을 가려낼 수 있을까?
유전자 치료, 치명적인 유전성 심근증의 대안이 될 수 있을까?
Safety and Preliminary Efficacy of AAVrh.10hPKP2 (LX2020) Gene Therapy in PKP2-Arrhythmogenic Cardiomyopathy
연구요약
유전성 심장 질환은 환자와 가족에게 예기치 못한 비극을 안겨주는 치명적인 위협이다. 특히 부정맥 유발성 심근증(Arrhythmogenic Cardiomyopathy, ACM)은 심근이 점진적으로 지방 섬유 조직으로 대체되며 치명적인 심실 부정맥과 급사(Sudden cardiac death, SCD)를 유발하는 파괴적인 질환이다. 그중 Plakophilin-2(PKP2) 유전자의 기능 상실 변이는 ACM의 가장 흔한 원인(약 70%)으로 꼽히며, 미국 내 약 6만 명의 환자가 영향을 받고 있다. 환자의 약 23%가 SCD로 첫 증상을 경험하며, 기존의 제세동기(Implantable Cardioverter-Defibrillator, ICD)나 약물 치료는 질환의 진행을 근본적으로 멈추지 못한다는 한계가 있었다.
이러한 절망적인 상황에서 유전적 결함을 근본적으로 교정하려는 시도가 스탠퍼드 대학의 Victoria Parikh 박사에 의해 과학적으로 증명되어 이번 ACC 2026에서 발표되었다. 이 연구는 ACM의 가장 흔한 원인인 PKP2 유전자 변이 환자를 대상으로 수행된 LX2020 유전자 치료제의 임상 1/2상(HEROIC-PKP2) 결과이다. 이번 연구에 앞서 LX2020은 비인간 영장류 모델에서 1x10^14vg/kg)의 고용량 투여시에도 심장 기능, 심전도, 조직학적 측면에서 어떠한 이상 반응도 관찰되지 않아 우수한 안전성 프로파일을 확보하였기 때문에 본 연구를 수행할 수 있었다1.
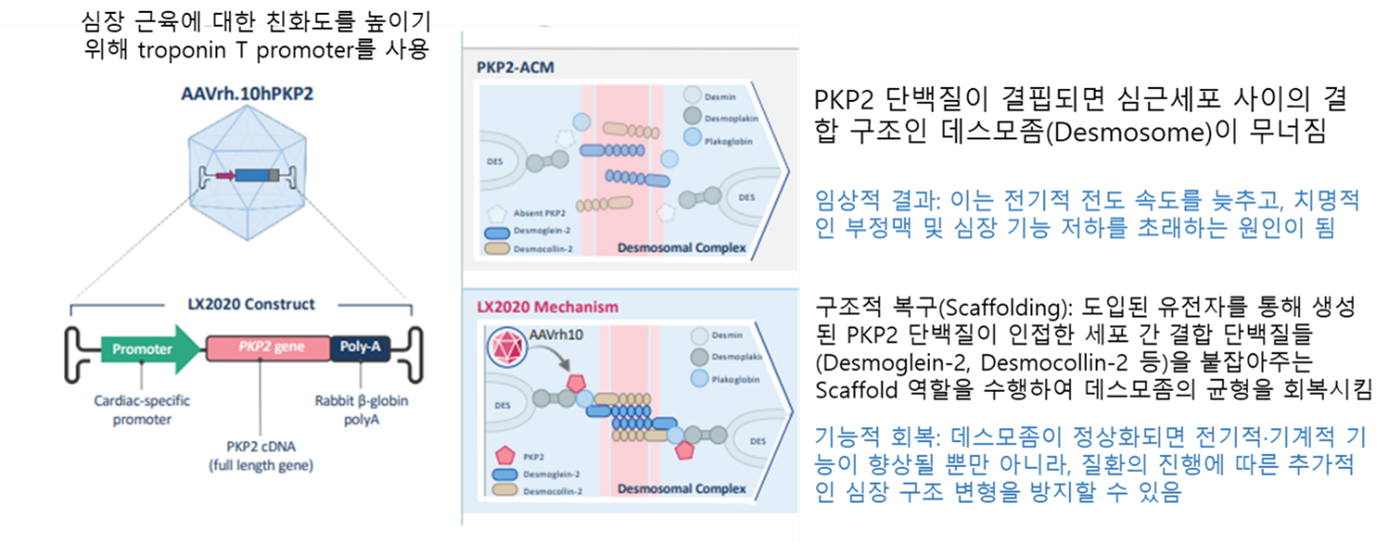
그림1. LX2020 virus construct와 작용 기전.
LX2020이 심근세포에 PKP2(Full-Length Plakophilin-2)를 전달하여 데스모솜(Desmosome, 세포 부착 구조)을 복원시킴
이번 연구는 ACM 환자 10명을 대상으로 저용량(2.0x10^13vg/kg)과 고용량(6.0x10^13vg/kg) 코호트로 나누어 수행되었다. 그 결과, LX2020은 심근세포에 정상적인 PKP2 유전자를 효과적으로 전달하여 무너진 세포 간 결합(데스모좀) 구조를 복구하는 것으로 나타났다(그림1).
주요 데이터에 따르면, 투여 3개월 후 시행한 심장 생검에서 고용량군 참가자들의 PKP2 단백질 발현이 평균 162%나 증가하였다. 이는 단순한 유전자 전달을 넘어, 실제 심장 기능을 지탱하는 단백질 scaffold가 성공적으로 복구되었음을 의미한다.
임상적 효능 또한 고무적이었다. 고용량 군 참가자의 다수에서 비지속성 심실 빈맥(NSVT)이 감소하거나 안정화되는 신호가 관찰되었으며, 환자들이 느끼는 주관적 증상 또한 전반적으로 개선되었다. 특히 5명 중 4명의 고용량 군 참가자가 증상의 호전을 보고하였다.
안전성 측면에서 일부 환자의 간 수치(LFT) 상승이 관찰되었고 한 명의 참가자에게서 지속성 심실 빈맥(VT)이 발생하기도 했으나, 이는 프로토콜에 따른 면역억제 조절 및 약물 치료를 통해 성공적으로 관리되었다. 중도 포기자 없이 모든 참가자가 연구를 지속하고 있다는 점은 이 치료법의 안정성이 확보되었음을 보여준다.
임상적 의의
이번 연구는 ACM의 근본 원인을 타겟팅하여 심장 내부의 전도 장애와 구조적 붕괴를 역전시킬 수 있는 가능성을 처음으로 제시하였다. 이는 단순한 증상 완화를 넘어 유전적 결함을 직접 교정하여 심장을 '정적 상태(Quiescence)'로 되돌리려는 시도가 실제 임상에서 유효함을 입증한 것이다. 우리가 인지하지 못한 사이 발전한 유전자 편집 기술은 이제 희귀 심장 질환 환자들에게 돌연사의 공포로부터 벗어날 수 있는 실질적인 희망을 제공하고 있다.
참고문헌
1) Jing Zhang et.al., Preclinical efficacy and safety of AAVrh10-based plakophilin-2 gene therapy (LX2020) as a treatment for arrhythmogenic cardiomyopathy. 2025 10(1):17. Regen Med.

